Es gibt keine Website-Inhalte zu Ihrer Suchanfrage.
Website-Inhalte
Sie haben sich erfolgreich abgemeldet.
Noch nicht registriert?
Onkologie
Ein Medikationsfehler ist definiert als jedes vermeidbare Ereignis, das zu einer unsachgemäßen Anwendung von Arzneimitteln oder zu einer Schädigung des Patienten führen kann, während das Arzneimittel unter der Kontrolle des medizinischem Fachpersonals, des Patienten oder einer anderen Person steht.1 Medikationsfehler lassen sich anhand der Art des Fehlers klassifizieren – etwa die Verwechslung des Patienten, eine falsche Dosierung, Infusionsgeschwindigkeit, Applikationsart oder Medikation. Fehler können in jeder Phase des Medikationsprozesses auftreten – von der Verordnung bis zur Applikation – und an jedem Ort, an dem Arzneimittel verabreicht werden.2
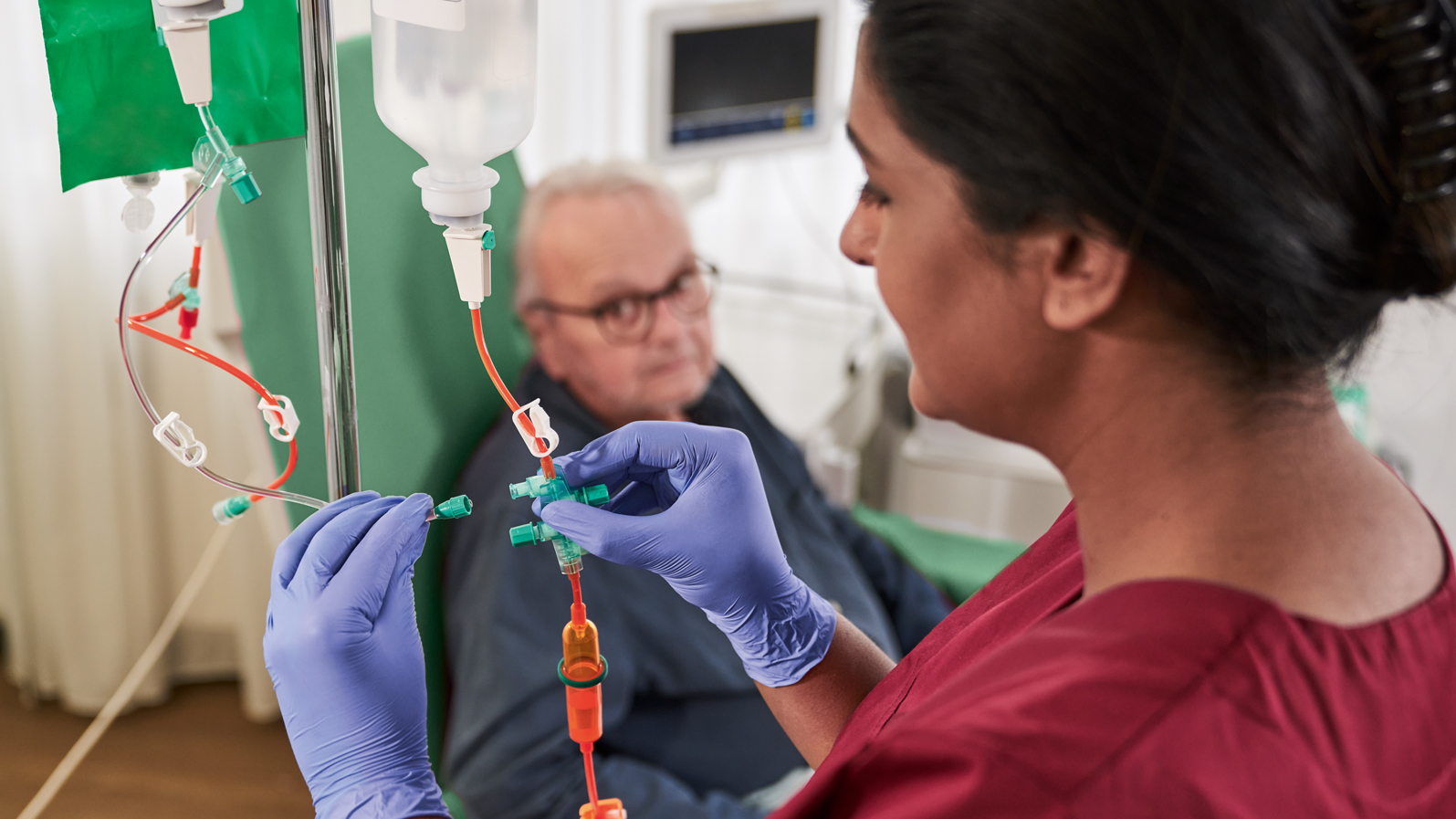
Grundsätzlich können alle medikamentösen Behandlungen betroffen sein. Die Chemotherapie birgt jedoch aufgrund enger therapeutischer Bereiche, potenzieller Toxizität selbst bei korrekter Dosierung, komplexer Behandlungsschemata und einer vulnerablen Patientengruppe besondere Gefahren.3
“Es mag Teil der menschlichen Natur sein, Fehler zu machen, aber es ist auch Teil der menschlichen Natur, Lösungen zu finden, bessere Alternativen zu entwickeln und sich den Herausforderungen zu stellen”
Frühere Studien legen nahe, dass Medikationsfehler einen erheblichen Anteil – wenn nicht sogar die Mehrheit – aller medizinischen Fehler und unerwünschten Ereignisse mit tödlichem Ausgang ausmachen.3 Damit bilden Medikationsfehler eine besonders relevante Untergruppe medizinischer Fehler – aufgrund ihrer Häufigkeit, ihres potenziellen Schadensausmaßes und ihrer prinzipiellen Vermeidbarkeit. Eine Untersuchung zeigte, dass Zytostatika die zweithäufigste Ursache tödlicher Medikationsfehler waren.4 Zudem gelten sie – nach Antiinfektiva – als die Arzneimittelklasse, die am häufigsten mit Medikationsfehlern assoziiert ist.5
39 % der Medikationsfehler betrafen Über- oder Unterdosierungen, 21 % Fehler bei der Dosierung und dem Zeitpunkt der Verabreichung, 18 % falsche Arzneimittel und 14 % eine Anwendung beim falschen Patienten. Seltener traten Fehler bei der Infusionsgeschwindigkeit, dem Nichtverabreichen von Medikamenten oder Flüssigkeitszufuhr sowie eine unsachgemäße Zubereitung auf. 10 % dieser Fehler erforderten eine medizinische Intervention und führten zu verlängerten Krankenhausaufenthalten.6
0%
betrafen Über- oder Unterdosierung
0%
betrafen Fehler bei der Dosierung und dem Zeitpunkt der Verabreichung
0%
betrafen falsche Arzneimittel
0%
betrafen die Verabreichung einer Chemotherapie beim falschen Patienten
Dosierungsfehler können in jeder Phase des Behandlungsprozesses auftreten. Über einen Zeitraum von zwei Jahren (2003–2004) führte Ford3 eine klinische Studie zu Medikationsfehlern auf der Onkologischen Station eines großen kommunalen Krankenhauses durch.
Insgesamt wurden 141 Fehler erfasst, davon 38 als „falsche Dosierung“ klassifiziert. Einer davon trat bei der Verordnung bzw. Dokumentation auf, 20 während der Herstellung und 17 bei der Verabreichung. Zusätzlich wurden 18 Fehler dokumentiert, bei denen Medikamente nicht verabreicht wurden.
In Adelaide (Australien) erhielten zwischen 2014 und 2015 zehn Krebspatient*innen über einen Zeitraum von sechs Monaten eine unzureichende Dosis des Medikamentes Cytarabin.4,7
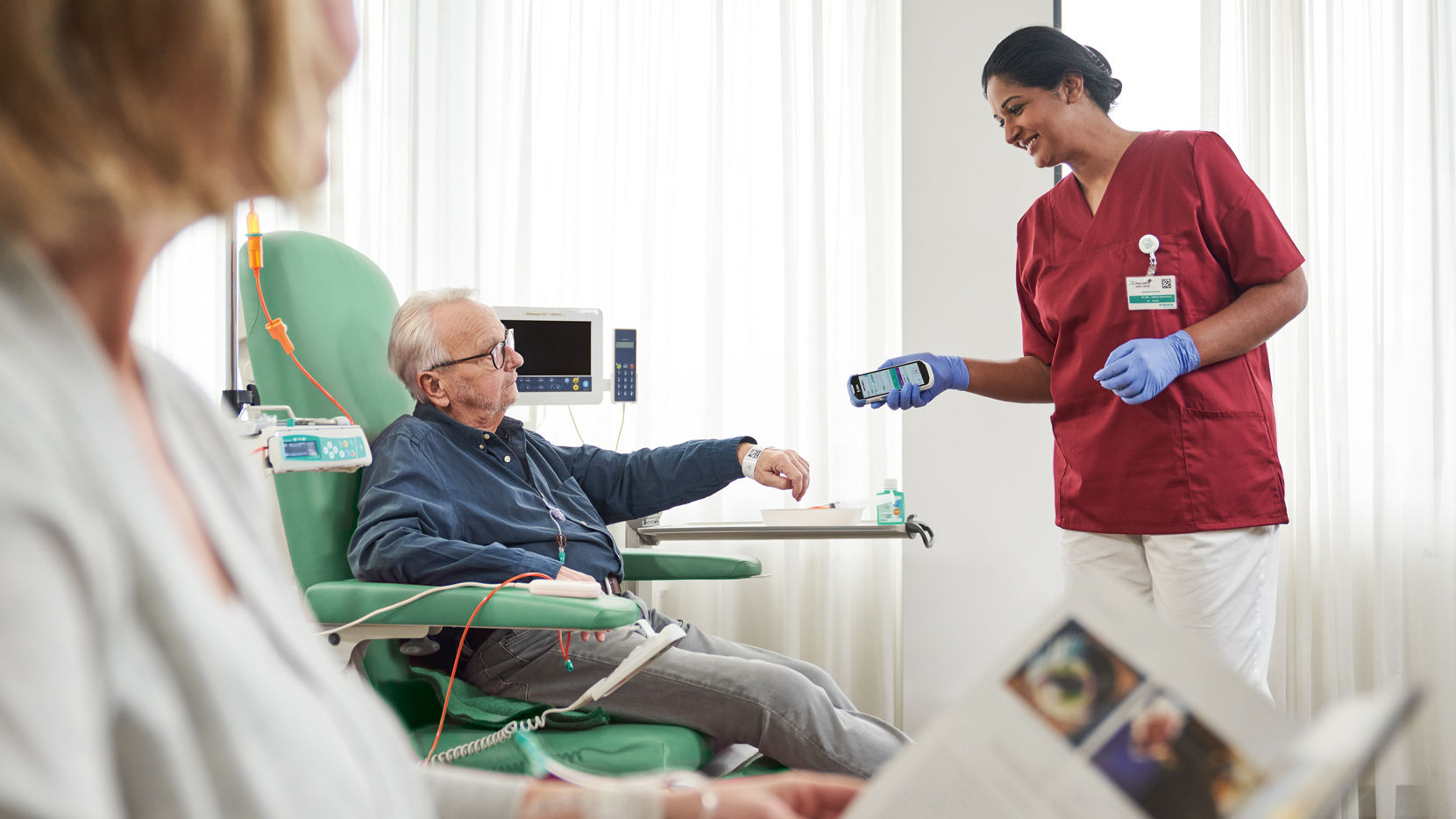
Mit OncoSafety Remote Control® werden die onkologische Behandlung und die Verabreichung von Chemotherapien digital verwaltet, kontrolliert und dokumentiert. Dies reduziert Risiken für Krebspatient*innen und hilft dem Pflegepersonal, Fehler bei der Verordnung, Zubereitung und Verabreichung von Zytostatika zu vermeiden.
0%
zu langsam verabreicht
0%
zu schnell verabreicht
0%
korrekt in der vorgeschriebenen Geschwindigkeit verabreicht
26 % wurden korrekt in der vorgeschriebenen Geschwindigkeit verabreicht
Die meisten Chemotherapien werden intravenös verabreicht, also direkt in das venöse System. Periphere Venenzugänge können geeignet sein – aufgrund der hohen Toxizität der Medikamente wird jedoch meist ein zentralvenöser Zugang bevorzugt.
Ein sechsjähriges Mädchen erhielt im Rahmen einer ambulanten Behandlung eine intrathekale Medikation. Drei Tage später stellte sie sich mit Schmerzen in Nacken und Beinen in der Notaufnahme vor.9
Einige Chemotherapie-Schemata erfordern alternative Zugangswege, etwa eine intraarterielle Gabe für isolierte Organperfusionen (z. B. bei Lebermetastasen) oder intrathekale Anwendungen – also Injektionen in den Spinalkanal über eine Lumbalpunktion.
Cytarabin (Ara-C) kann intrathekal bei karzinomatöser Meningitis im Rahmen eines Lymphoms oder einer Leukämie verabreicht werden; Methotrexat wird intrathekal bei karzinomatöser Meningitis infolge eines Brust- oder Bronchialkarzinoms eingesetzt.10
Ein Beispiel: Ein Patient mit hochmalignem Non-Hodgkin-Lymphom und karzinomatöser Meningitis erhält in der Regel Vincristin 2 mg i.v. plus Methotrexat 10–15 mg intrathekal.
Bestimmte Krebserkrankungen können zu Metastasen an den Hirnhäuten führen – in diesem Fall spricht man von karzinomatöser Meningitis. Sie tritt häufig bei Patient*innen mit Leukämie oder Lymphomen auf, aber auch bei Brustkrebs, Bronchialkarzinomen oder malignem Melanom.
Patient*innen mit soliden Tumoren und karzinomatöser Meningitis haben eine ungünstige Prognose. Ohne Behandlung beträgt die durchschnittliche Überlebenszeit meist nur wenige Wochen.
Vincristin ist ein Vincaalkaloid und ausschließlich intravenös zu verabreichen. Eine subkutane, intramuskuläre oder intrathekale Anwendung ist kontraindiziert, da sie zu Nekrosen führt.9
Eine versehentliche intrathekale Gabe von Vincristin – etwa über eine Lumbalpunktion oder ein Ommaya-Reservoir – verursacht schnell sensorische und motorische Ausfälle, gefolgt von Enzephalopathie, Koma und Tod.11
Bei Kombinationstherapien muss daher sichergestellt sein, dass jede Substanz über den dafür vorgesehenen Zugangsweg appliziert wird.
Die Verabreichung von Arzneimitteln über den falschen Applikationsweg – wie etwa die intrathekale Gabe von Vincristin oder die intravenöse Verabreichung von Benzathin-Penicillin (einer Depotformulierung zur intramuskulären Anwendung) – machen rund 5 % aller Medikationsfehler aus.
Die besonderen Risiken einer Fehlanwendung von Vincristinsulfat sind bereits seit den ersten klinischen Erfahrungen in den 1960er-Jahren bekannt.13 Dennoch sind seither 58 Fälle intrathekaler Vincristin-Applikationen dokumentiert, die umfassend ausgewertet wurden.12, 9
Nur acht der betroffenen Patient*innen überlebten – die meisten von ihnen gelähmt.14 Einzelne Fallberichte wurden veröffentlicht.9, 14, 15
Vorkehrungen zur Vermeidung der intrathekalen Verabreichung bestimmter Arzneimittel16
Die meisten Krankenhäuser haben klare Sicherheitsvorgaben etabliert, um die versehentliche intrathekale Verabreichung von Vincristin und anderen Vinca-Alkaloiden zu verhindern. Am Great Ormond Street Hospital for Children in London gelten beispielsweise folgende Regeln:
Der universelle Luer-Konnektor wurde als wesentlicher Risikofaktor für Fehlapplikationen identifiziert. Luer-Verbindungen werden häufig für die Verabreichung von Infusionen verwendet – gleichzeitig zeigen Studien, dass Patient*innen mit mehreren Zugangssystemen einem erhöhten Risiko für Fehlapplikationen ausgesetzt sind.17
Um das Risiko von Medikationsfehlern im Rahmen von Chemotherapien zu senken, hat die Internationale Organisation für Normung (ISO) verbindliche Standards für Konnektoren mit kleinen Durchmessern entwickelt – unter anderem für neuraxiale und regionale Anästhesieverfahren (ISO 80369-6).
Produkte, die dieser Norm entsprechen, tragen die Bezeichnung NRFit®. Sie sind 20 % schmaler als Luer-Verbindungen und verfügen über eine gelbe Farbcodierung.18
Mehr erfahren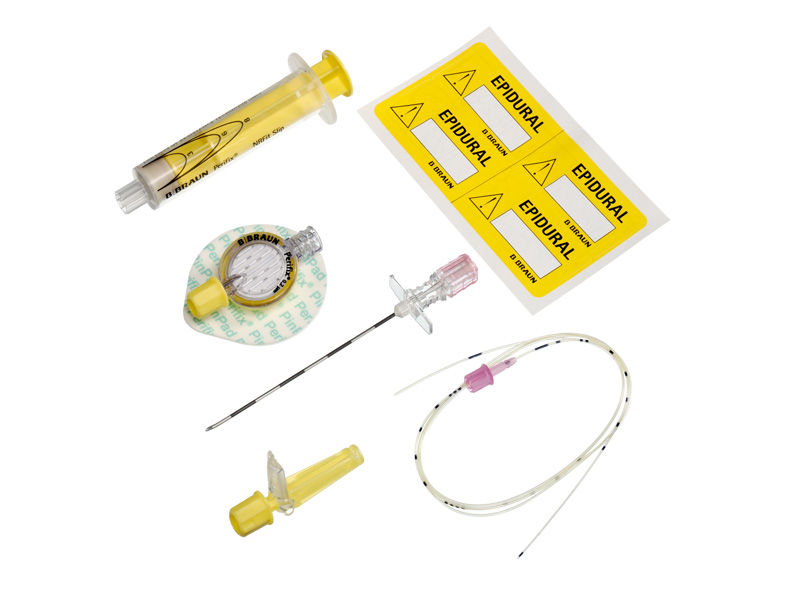
Fehler verursachen auch erhebliche indirekte Kosten. Mittel, die für die Wiederholung von Untersuchungen oder die Behandlung unerwünschter Arzneimittelwirkungen aufgewendet werden, fehlen an anderer Stelle. Patient*innen und Einkäufer zahlen doppelt – etwa durch höhere Versicherungsbeiträge oder Zuzahlungen für Leistungen, die bei fehlerfreier Versorgung nicht notwendig gewesen wären.
Doch nicht alle Kosten lassen sich beziffern: Medikationsfehler in der Chemotherapie führen auch zu Vertrauensverlust, einer geringeren Patientenzufriedenheit und Frustration beim Pflegepersonal.
Patient*innen zahlen mit körperlicher und seelischer Belastung durch verlängerte Klinikaufenthalte oder bleibende Einschränkungen.
Medizinisches Fachpersonal zahlt mit dem Verlust an Motivation, wenn die Versorgung hinter dem eigenen Anspruch zurückbleibt.
Und auch die Gesellschaft trägt die Last – durch Produktivitätsverluste, Fehlzeiten in Schule und Beruf und einem schlechteren Gesundheitszustand der Bevölkerung.19
| Krankenhausaufenthalte | 62.248 € |
| Zusätzliche Medikamente | 23.658 € |
| Gesamtkosten pro Jahr | 92.248 € |
“Primum nil nocere.”
„Es mag Teil der menschlichen Natur sein, Fehler zu machen, aber es ist auch Teil der menschlichen Natur, Lösungen zu finden, bessere Alternativen zu entwickeln und sich den Herausforderungen zu stellen.“
In ihrer wegweisenden Veröffentlichung aus dem Jahr 1999 riefen Kohn und Kollegen vom Institute of Medicine (IOM) den gesamten Gesundheitssektor zum Handeln auf.19 Das IOM-Gremium forderte einen grundlegenden Wandel im Verständnis medizinischer Fehler, indem Prinzipien aus der kognitiven Psychologie und den Human Factors, der Untersuchung der menschlichen Leistungsfähigkeit in Arbeitsumgebungen, angewendet werden. Beispiele aus der Luftfahrt, der chemischen Industrie, der Produktion und der Kerntechnik zeigten: Nicht der einzelne Behandelnde, sondern das System ist häufig die eigentliche Fehlerquelle – und zugleich der Ansatzpunkt für Verbesserungen durch Vereinfachung, Standardisierung und Technologie.21,30
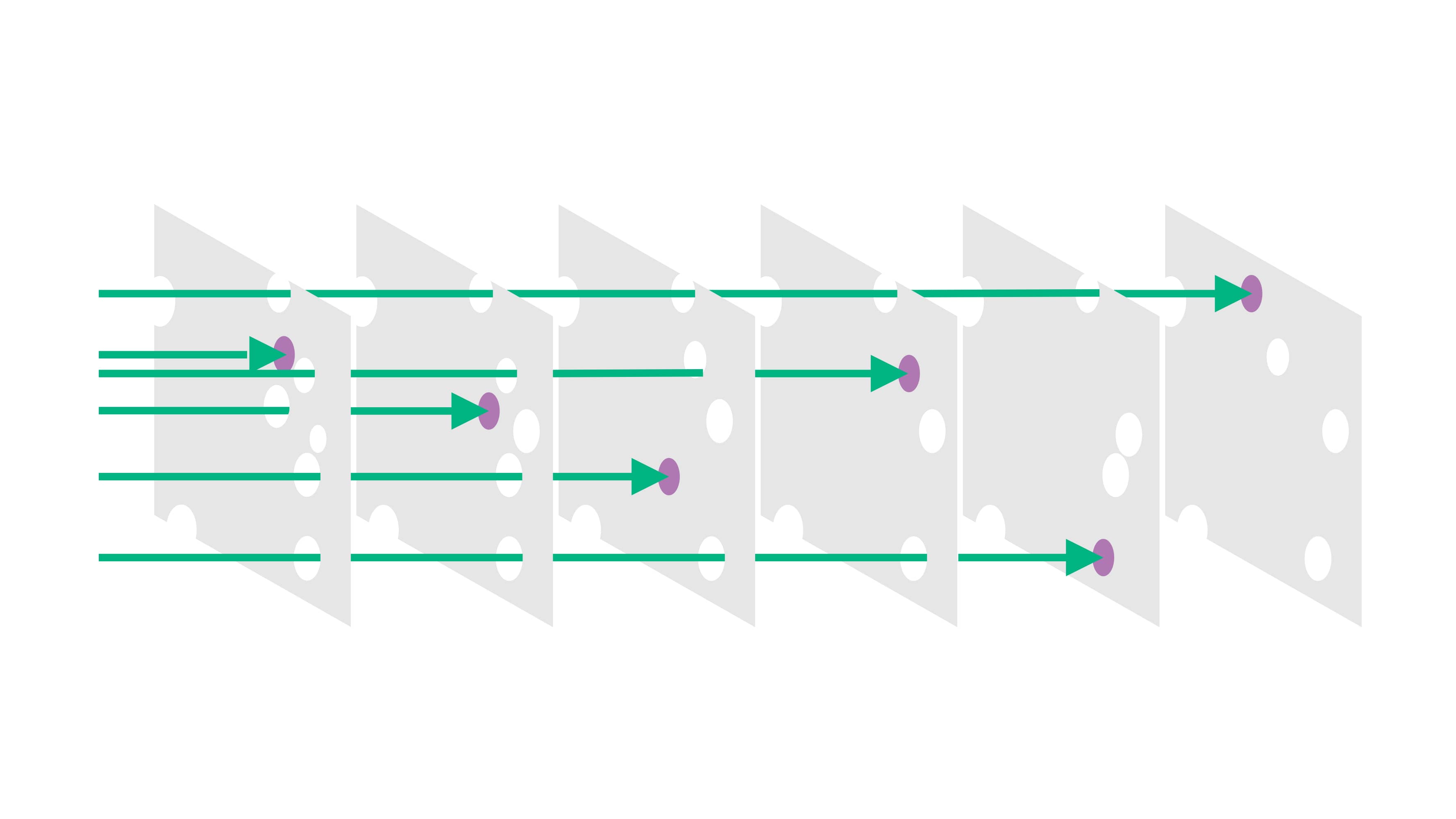
Im selben Jahr wurde dieses Prinzip als „Swiss-Cheese-Modell“ bekannt: Mehrere Sicherheitsebenen sollen verhindern, dass Fehler (Löcher im Käse) bis zum Patienten durchdringen.22, 29 Dieses Modell bildet seither die konzeptionelle Grundlage für Critical Incident Reporting Systems (CIRS) – also Systeme zur Meldung und Analyse von kritischen Ereignissen und Beinahe-Fehlern mit dem Ziel, daraus systematisch zu lernen.
Die American Society of Health-System Pharmacists (ASHP) entwickelte bereits 2002 eine Richtlinie zur Vermeidung von Medikationsfehlern bei Chemo- und Biotherapien, die inzwischen aktualisiert wurde.20
Die Guideline enthält Empfehlungen für Gesundheitseinrichtungen, für ein interdisziplinäres Monitoring und die Verifizierung des Medikationsprozesses, für Verordnungssysteme und Verschreibende, für die Zubereitung und Abgabe durch Apotheken, für die Verabreichung durch Pflegefachkräfte sowie für die Patientenaufklärung. Darüber hinaus richtet sie sich auch an Hersteller, Aufsichtsbehörden und beschreibt Strategien zum Erkennen und Management von Medikationsfehlern.

Krankenschwester, Abteilung für Onkologie und Hämatologie am Hospital San Pau i Santa Creu in Barcelona, Spanien
Fehler in der Applikationstechnik können verschiedene Aspekte der Infusion betreffen. Ein Beispiel:
Paclitaxel ist ein häufig eingesetztes Chemotherapeutikum zur Behandlung von Brust-, Ovarial- und Bronchialkarzinomen. Der Wirkstoff neigt zur Bildung von Mikroluftblasen und Partikeln. Laut Fachinformation (SmPC Paclitaxel) empfehlen die Hersteller daher die Anwendung eines Inline-Filters während der Infusion. Wird dieser Filter nicht verwendet, können Partikel in den Patienten gelangen.37
Partikel aus der Infusionstherapie können inflammatorische Prozesse auslösen oder verstärken. Sie gelten als Auslöser für Thrombosen, beeinträchtigen die Mikrozirkulation und beeinflussen das Immunsystem.
Partikelquellen sind unter anderem Materialien der Infusionssysteme, unvollständig rekonstituierte Lösungen oder Inkompatibilitätsreaktionen.
Schätzungen zufolge können pro Patient*in und Tag bis zu eine Million Partikel infundiert werden. Inline-Filter in Infusionsleitungen halten diese Partikel zurück – und verhindern so nahezu vollständig deren Eintritt.41
Weitere Risiken ergeben sich durch ein fehlerhaftes Zusammensetzen von Infusionssystemen für Sekundärinfusionen (mit oder ohne Pumpe), versehentlich offen gelassene Luer-Zugänge oder Nadelstichverletzungen durch manuelle Manipulation mit Nadeln.
Vorfälle, bei denen Patient*innen falsch identifiziert werden – sogenannte „Wrong Patient“-Fehler – sind in der onkologischen Praxis nicht unbekannt. Viele dieser Ereignisse bleiben Beinahe-Fehler oder werden in letzter Minute erkannt, bevor es zur Verabreichung kommt. Die tatsächliche Häufigkeit ist unbekannt, da Patientenverwechslungen häufig nicht gemeldet werden.38
Eine Pflegekraft bat Frau Jackson, zum Chemotherapie-Raum in der onkologischen Praxis zurückzukehren …41
Bereits 2002 definierte die Joint Commission im Rahmen ihres Programms zu nationalen Patientensicherheitszielen die korrekte Identifikation des Patienten als oberste Priorität. Um diesem Ziel gerecht zu werden, verwenden Pflegefachkräfte mindestens zwei Patientenmerkmale – in der Regel Name und Geburtsdatum.
Die American Society of Clinical Oncology (ASCO) und die Oncology Nursing Society entwickelten gemeinsam Sicherheitsstandards für die Verabreichung von Chemotherapie bei erwachsenen Patient*innen. Ziel ist es, Fehler zu vermeiden und Best-Practice-Strukturen in der onkologischen Versorgung zu fördern.39, 35
Auf einen Blick:42
Patientenverwechslungen können in nahezu jeder Phase des Behandlungskontaktes auftreten
Sicherheitssysteme können „Wrong Patient“-Fehler reduzieren, aber nicht vollständig ausschließen – denn auch sie sind anfällig für menschliches Versagen
Eine korrekte Patientenidentifikation beginnt bereits bei der Anmeldung
1. National Coordinating Council for Medical Error Reporting and Prevention (NCCMERP): What is a Medication Error. available at: https://www.nccmerp.org/about-medication-errors; accessed 02-23-2023.
2. The Boston Globe, 2004
3. Ford et al (2006): Study of Medication Errors on a Community Hospital Oncology Ward. Journal of Oncology Practice, 2006, 2 (4), 149-154. available at: https://ascopubs.org/doi/full/10.1200/jop.2006.2.4.149; accessed 02-23-2023.
4. ABC. (2015): South Australian Government launches inquiry over chemotherapy drug-dosing bungle. [online] available at: http://www.abc.net.au/news/2015-08-05/sa-government-launches-inquiry-over-chemotherapy- ungle/6673890; accessed 02-23-2023.
5. Lustig A. (2000): Medication error prevention by pharmacists – an Israeli solution. Pharmacy World and Science. 2000, 22 (1), 21–25.
6. Schulmeister L. (1999): Chemotherapy medication errors: descriptions, severity, and contributing factors. Oncol Nurs Forum. 1999; 26(6):1033-42.
7. MacIennan, L. (2016): Chemotherapy bungle at Adelaide hospitals due to clinical failures, SA Health Minister says. [online] available at: http://www.abc.net.au/news/2016-02-09/chemotherapy-bungle-at-adelaide-hospitals-under-review/7153168 accessed: 02-23-2023
8. Rooker JC, Gorard DA (2007): Errors of intravenous fluid infusion rates in medical inpatients. Clin Med. 2007;7: 482–5. available at: https://pdfs.semanticscholar.org/ec0d/acd06790eef073fb64a0678b74ca065e0516.pdf; accessed: 02-23-2023.
9. Hennipmann B. et al (2009): Intrathecal Vincristine. 3 Fatal Cases and a Review of the Literature. Journal Pediatric Hematol Oncol. 2009, 31 (11), 816-819.
10. Schulmeister L. (2006): Look-alike, sound-alike oncology medications. Clin J Oncol Nurs 2006, 10(1):35-41.
11. Bates DW et al (1995): Relationship between medication errors and adverse drug events. J Gen Intern Med 1995;10 (4):199-205
12. Noble D. (2010): The quest to eliminate intrathecal vinchristine errors: a 40-year journey. BMJ Quality & Safety 2010, 19, 323-326.
13. Toft B (2001): External Inquiry into the adverse incident that occurred at Queen’s Medical Centre, Nottingham, 4th January 2001, [online]. Available at: https://webarchive.nationalarchives.gov.uk/ukgwa/20080728185547/http://www.dh.gov.uk/en/Publications accessed: 02-23-2023
14. Arzneimittelkommission der deutschen Ärzteschaft (2005): Vincristin: Toedliche Zwischenfaelle nach versehentlicher intrathekaler Gabe. Deutsches Aerzteblatt 2005, 102,1615.
15. Dyer c (2001): Doctors suspended after injecting wrong drug into spine. BMJ 2001, 322 (7281). 257.
16. Kress R. et al. (2016): Unintentional Infusion of Phenylephrine into the Epidural Space. A&A Case Rep. 2016, 6(5),124-7.
17. International Organization for Standardization (2016): Small bore connectors for liquids and gases in healthcare applications -- Part 6: Connectors for neuraxial applications. [online] available at: https://www.iso.org/standard/50734.html accessed: 02-23-2023
18. Institute for Safe Medication Practices (2014): ISMP List of High-Alert Medications in Acute Care Settings [online] available at: https://www.ismp.org/sites/default/files/attachments/2018-01/highalertmedications%281%29.pdf accessed 06-07-2019
19. Ranchon et al. (2011): Chemotherapeutic errors in hospitalised cancer patients: attributable damage and extra costs. BMC Cancer 2011, 11:478.
20. Sasse M. et al. (2015): In-line Filtration Decreases Systemic Inflammatory Response Syndrome, Renal and Hematologic Dysfunction in Pediatric Cardiac Intensive Care Patients. Pediatric Cardiology 2015, 36 (6),1270–1278.
21. Reason, James (2000-). Human error: models and management. BMJ, 320 (7237): 768–770.
22. Weingart SN (2018): Chemotherapy medication errors. Lancet Oncol 2018, 19 (4), 191–99.
23. Parshuram CS, To T, Seto W, Trope A, Koren G, Laupacis A (2008) Systematic evaluation of errors occurring during the preparation of intravenous medication. CMAJ; 178(1): 42-8.
24. Cousins DH, Sabatier B, Begue D, Schmitt C, Hoppe-Tichy T (2005) Medication errors in intravenous drug preparation and administration: a multicentre audit in the UK, Germany and France. Qual Saf Health Care; 14(3): 190-5.
25. Taxis K, Barber N,(2003) Etnographic study of incidence and serverity of intravenoius drug errors. BMJ 326:684
26. Dehmel C, Braune S, Keymann G, Baehr M, Langebrake C, Hilgarth H, Nierhaus A, Dartsch D, Kluge S (2011) Do centrallly pre-pared solutions achieve more reliable drug concentrations than solutions prepared on the ward? Intensive Care Med 2010-00231. R3 in press.
27. Tissot E. Cornette C, Limat S, Maourand J, Becker M, Etievent J et al. (2003) Observational study of potential risk factors of medication administration errors. J Qual Improve 25(6):264-68
28. Vogel Kahmann I, Bürki R et al. (2003) Incompatibility reactions in the intensive care unit. Five years after implementation of a simple "color code system". Anasthesist 52(5):409-12
29. Valentin A, Capuzzo M, Guidet B, Moreno R, Metnitz B, Bauer P et al. (2009). Errors in adminstration of parental drugs in intensive care units: multinational prospective study. BMJ 338:b814. doi:10.1136/bmj.b814
30. Langebrake C, Hilgarth H (2010) Clinical pharmacists' interventions in a German University Hospital. Pharm World Svi 32(2):194-99
31. Taxis K (2005) Who is responsible for the safety of infusion devices? It's high time for action! QSHC 14(2):76
32. Rothschild JM, Keohane CA, Thompson S, Bates DW (2003) Intelligent Intravenous Infusion Pumps to improve Medication Administration Safety. AMIA Symposium Proceedings, p.992
33. Trissel LA (2011). Handbook on Injectable Drugs. 16th ed. Bethesda: American Society of Pharmacist.
34. Brigss J (2005) Strategies to reduce medication errors with reference to older adults. Best practice 9(4):1-6
35. Irajpour A, Farzi S, Saghaei M, Ravaghi H. Effect of interprofessional education of medication safety program on the medication error of physicians and nurses in the intensive care units. J Educ Health Promot. 2019 Oct 24;8:196.
36. Kane-Gill SL, Jacobi J, Rothschild JM (2010) Adverse drug events in intensive care units: Risk factors, impact and the role of team care. Crit Care Med 38(6): 83-89
37. Etchells E, Juurllink D, Levinson W (2008) Medication Errors: the human factor. CMAJ 178(1):63
38. Huckels-Baumgart S, Baumgart A, Buschmann U, Schüpfer G, Manser T. Separate Medication Preparation Rooms Reduce Interruptions and Medication Errors in the Hospital Setting: A Prospective Observational Study. J Patient Saf. 2021 Apr 1;17(3):e161-e168.
39. Smeulers M, Verweij L, Maaskant JM, de Boer M, Krediet CT, Nieveen van Dijkum EJ, Vermeulen H. (2015) Quality indicators for safe medication preparation and administration: a systematic review. PLoS One. 2015 Apr 17;10(4):e0122695. doi: 10.1371
40. Jones JH, Treiber L (2010) When 5 rights Go Wrong. J Nurs Care Qual 25:240-247
41. Schulmeister L (2007): Patient Misidentification in Oncology. Clinical Journal of Oncology Nursing 2007, 12 (3), 495-498. Available at: https://cjon.ons.org/cjon/12/3/patient-misidentification-oncology-care accessed: 02-23-2023
42. Schulmeister L (2002): Searching for Information for Presentations and Publications. Clinical Nurse Specialist, 2002, 16 (2); 79-84
43. Goldspiel B, Hoffman JM, Griffith NL, et al. ASHP guidelines on preventing medication errors with chemotherapy and biotherapy. Am J HealthSyst Pharm. 2015; 72:e6–35